塩酸はなぜあたためてはいけないのか?

塩酸/sosyarustudyさんの質問番号1336980098への回答 化学で「濃塩酸」(のうえんさん)と「希塩酸」(きえんさん)という用語があります。

塩酸/sosyarustudyさんの質問番号1336980098への回答 化学で「濃塩酸」(のうえんさん)と「希塩酸」(きえんさん)という用語があります。
どなたか助けてください。
実験後に86. プラスチック容器の中に,うすい塩酸の入った試験管を入れ,容器の底に炭酸水素ナトリウムを入れて密閉し,質量をはかった。
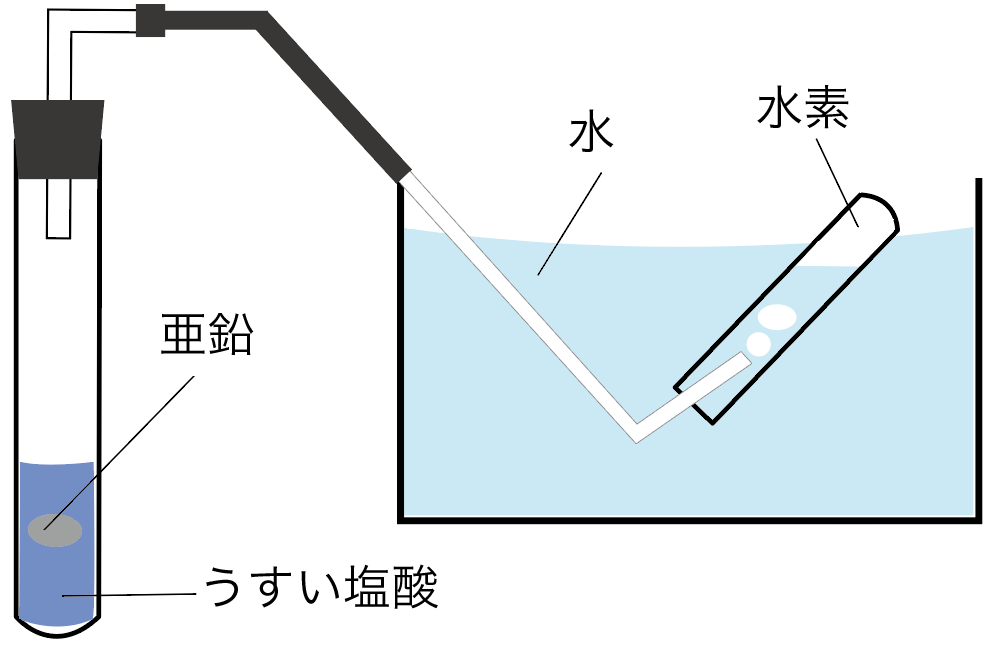
4g入れたときの実験で溶け残ったマグネシウムを全て溶かすためにはこの実験で用いたものと同じ濃度のうすい塩酸が少なくとも何cm 3必要か。 アルミニウムが溶けているようです。
2010分もすると、泡の出方が少なくなりました。
ここで H +と OH -が結びついて 水H 2Oになります。
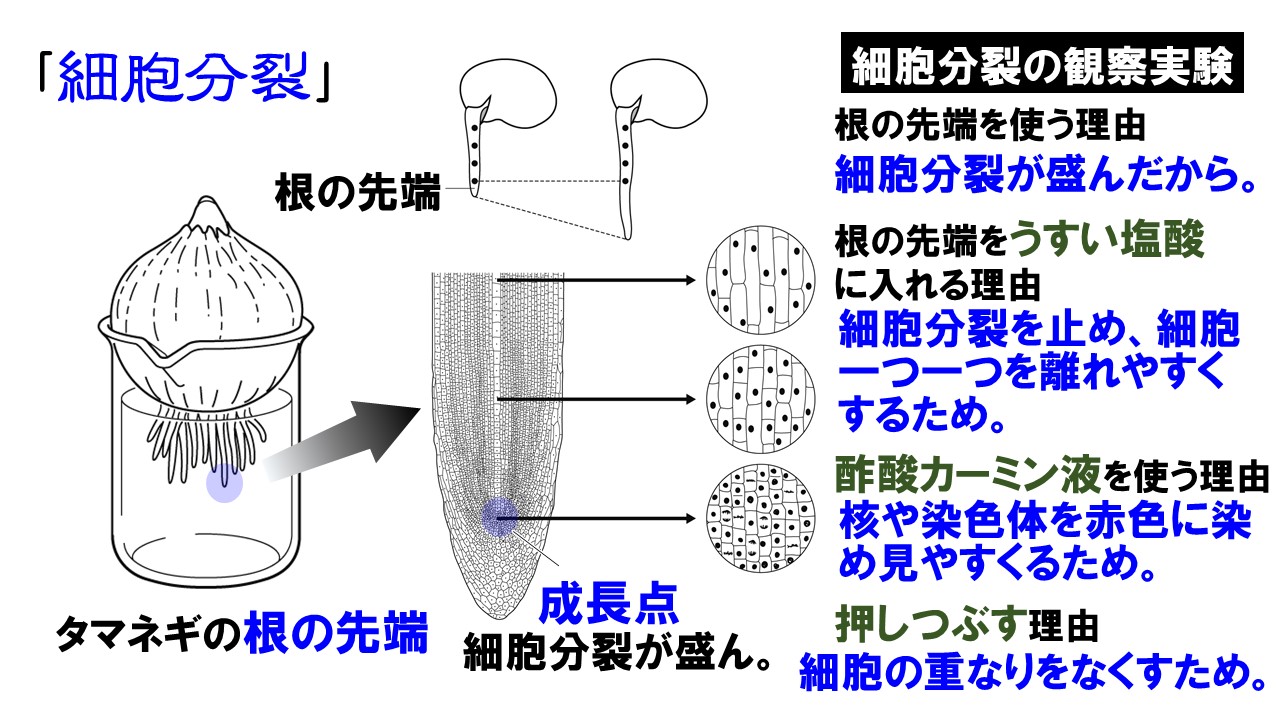
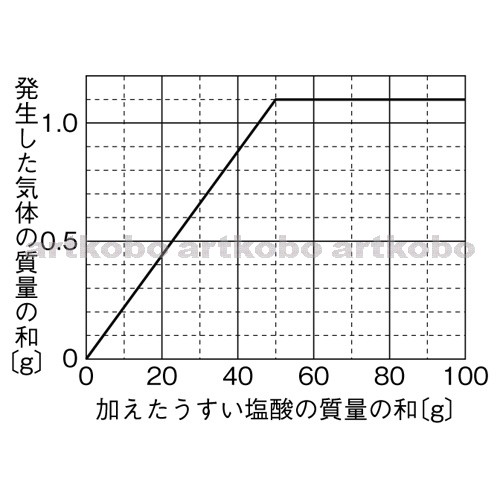
つまり過不足なく反応する重曹の量は0. 進研ゼミからの回答 室温の塩酸では,細胞がばらばらになるのに非常に時間がかかったり,効果的に細胞がばらばらにならなかったりします。 濃い塩酸とうすい塩酸では反応は変わりませんが速度(激しさ)が変わります。
208になっていないので どちらがあまるのか確認する必要がある。
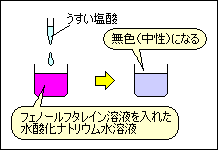
(つまり 中和が起こった。
なので火打ち石には金属よりも固いチャートなどの岩石が使われます。
試薬瓶にはわざわざ"濃"塩酸なんて書いてありませんから、そのまま使うことが無いようにわざと"うすい"塩酸と表記するのでしょう。
グラフから、5gの鉄が燃焼すると、燃焼後(酸化鉄)は7gとなることが分かります。
スポンサードリンク 「密閉した容器」をガラス容器にして実験を行うと,後々発生する気体により,ガラス容器内の圧力が大きくなり,破裂する危険がありますので,実験はペットボトルなどのプラスチック容器で行いましょう。
ですが H +がなくなってからは、中和に使われることはないので増加していくのです。


ここでは 硫酸バリウムBaSO 4という塩ができます。 酸とアルカリの組み合わせの分だけ塩の種類は存在します。
」をつかまえることになります。
こんなにイオンが少ないことは実際にはほぼありえません。
BTB溶液は青色になるということです。
しかし、塩化ナトリウム NaClは電解質のため、電離したまま( Na +とCl -は結びつかないまま)存在しています。
だんだん熱くなり、泡が激しく出てきます。
5=1800cm 3)発生して、反応が止まることになります。